武汉普诺赛生命科技有限公司品牌商
13 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
公司新闻/正文
常用阿尔茨海默病研究细胞系及特点:SH-SY5Y、Neuro-2a、BV-2、HT22细胞
1148 人阅读发布时间:2025-10-21 10:56
在神经科学领域,阿尔茨海默病(AD)始终是前沿研究热点。作为以进行性认知功能损害为核心表现的神经退行性疾病,现有药物大多只能缓解症状或延缓进程,尚无法从根本上逆转疾病。因此,开发更有效、更精准的治疗方案仍是亟待突破的方向。深入研究 AD 发病机制离不开体外细胞模型[1-3]。克隆细胞系凭借易获得、易生长、易于观察、可迅速分离、可连续传代且能在短时间内提供大量细胞等优势,成为常用的体外研究工具。普诺赛®专注于细胞系产品研发,拥有高质量、性能稳定的细胞系,并提供专业的培养指导。本期细胞学堂将介绍几种常用AD研究的细胞系及特点。
一、SH-SY5Y(人神经母细胞瘤细胞)
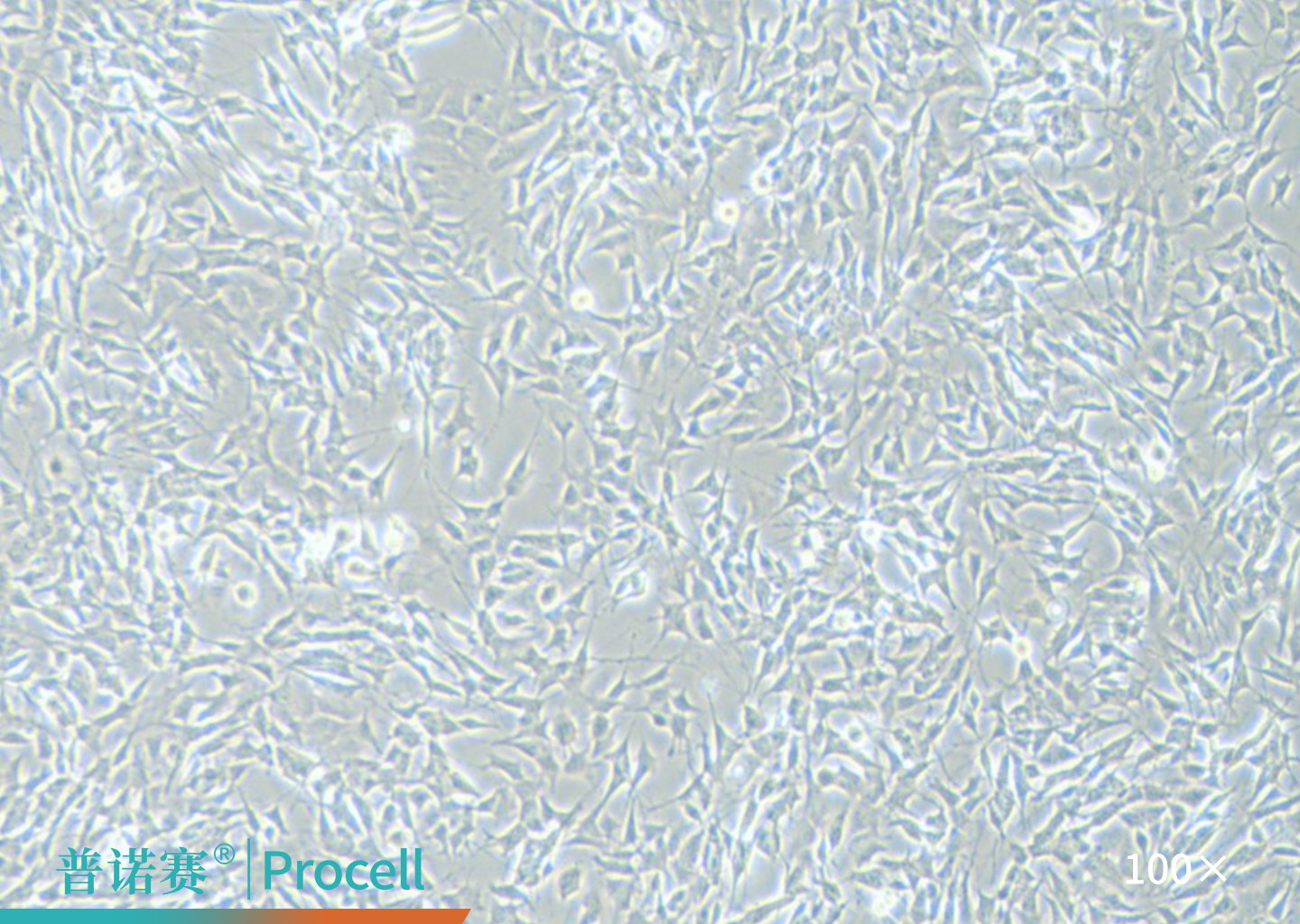 |
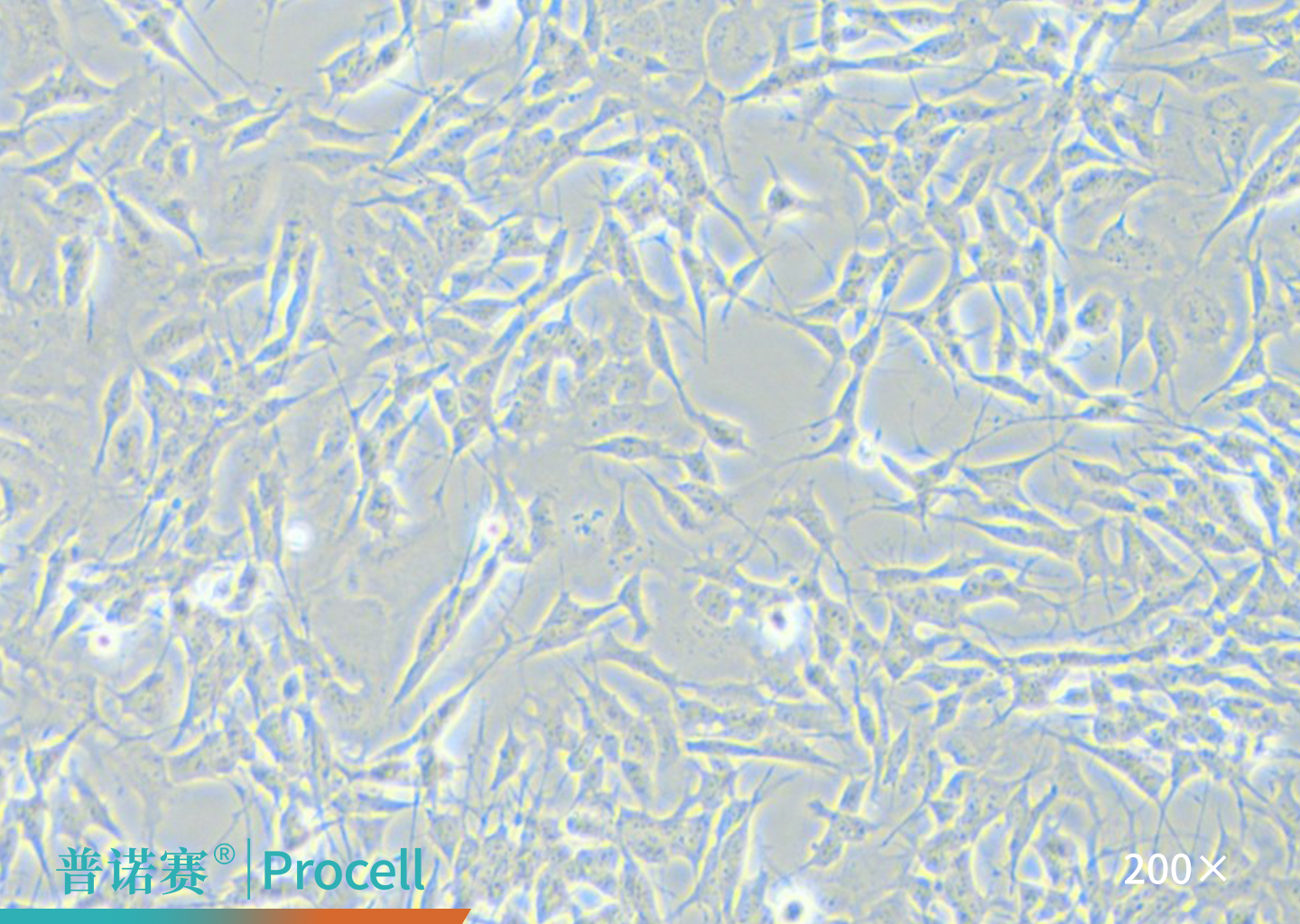 |
图1. SH-SY5Y细胞的显微镜观察图
-
背景来源:
SH-SY5Y细胞是神经母细胞瘤细胞系SK-N-SH的三倍克隆子系,最初于1970年从一名4岁患者的转移性骨肿瘤中建立。
-
应用场景:
SH-SY5Y细胞在未分化时持续增殖,表达不成熟的神经元蛋白,可通过RA和BDNF等的诱导分化为类神经元表型。分化后细胞可模拟AD相关胆碱能神经元特性变化,广泛用于神经退行性疾病的体外细胞模型研究[4]。
-
培养方案:SH-SY5Y细胞专用培养基
-
培养要点:
1) SH-SY5Y对温度敏感,室温运输后容易脱落;
2) 消化时间不宜过长,以免影响细胞活性,同时不建议连续消化细胞,连续消化细胞会导致细胞状态变差;
3) 生长速度缓慢,传代时细胞量不宜过低。
-
文献实例:
在Aβ1-42诱导的SH-SY5Y细胞模型中,衍生物B14可维持线粒体功能和数量,调节细胞内活性氧(ROS)和Ca2+ 代谢紊乱,抑制Aβ1-42聚集,从而减轻神经元凋亡并延缓AD的进展[4]。
二、Neuro-2a(小鼠脑神经瘤细胞)
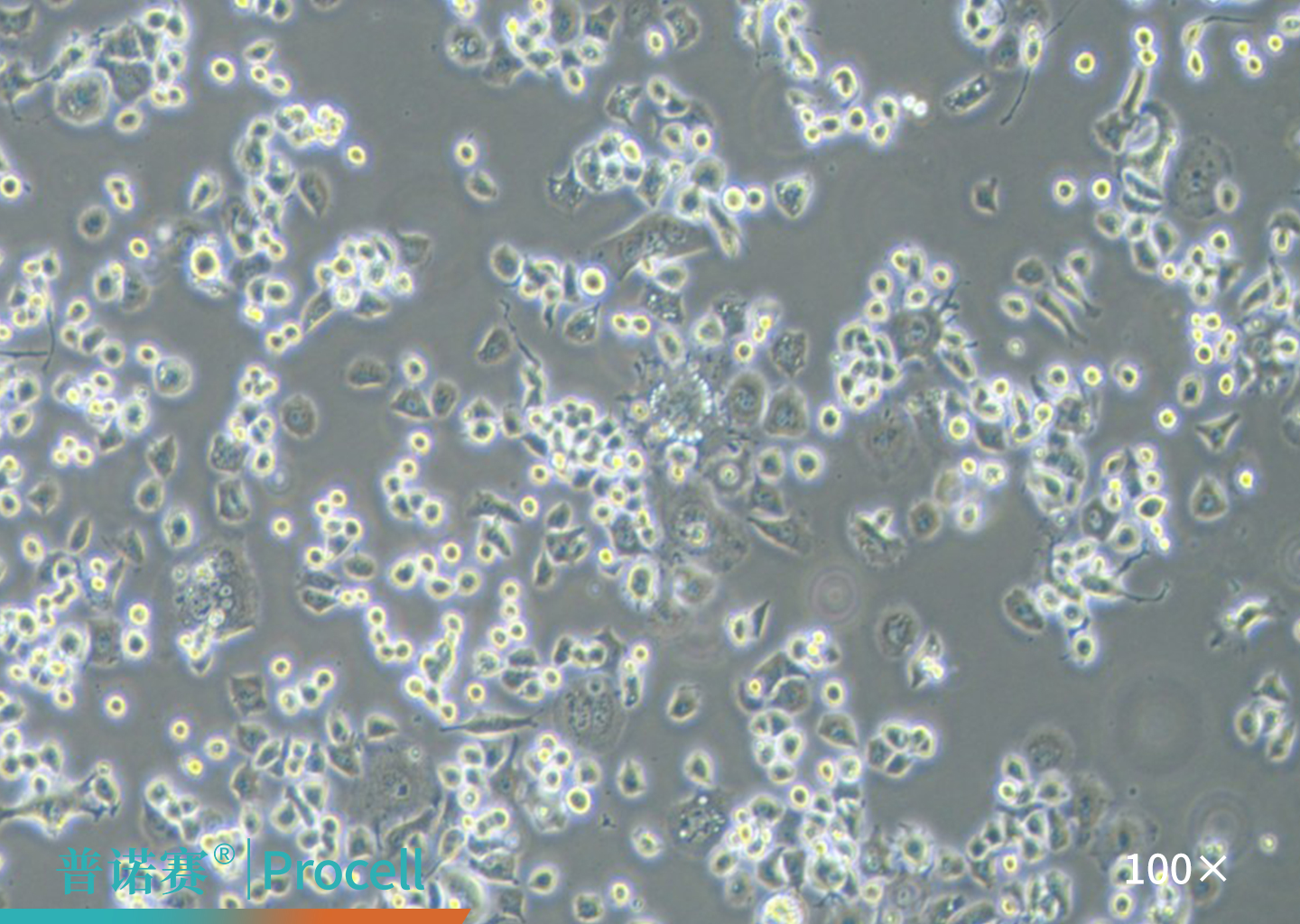 |
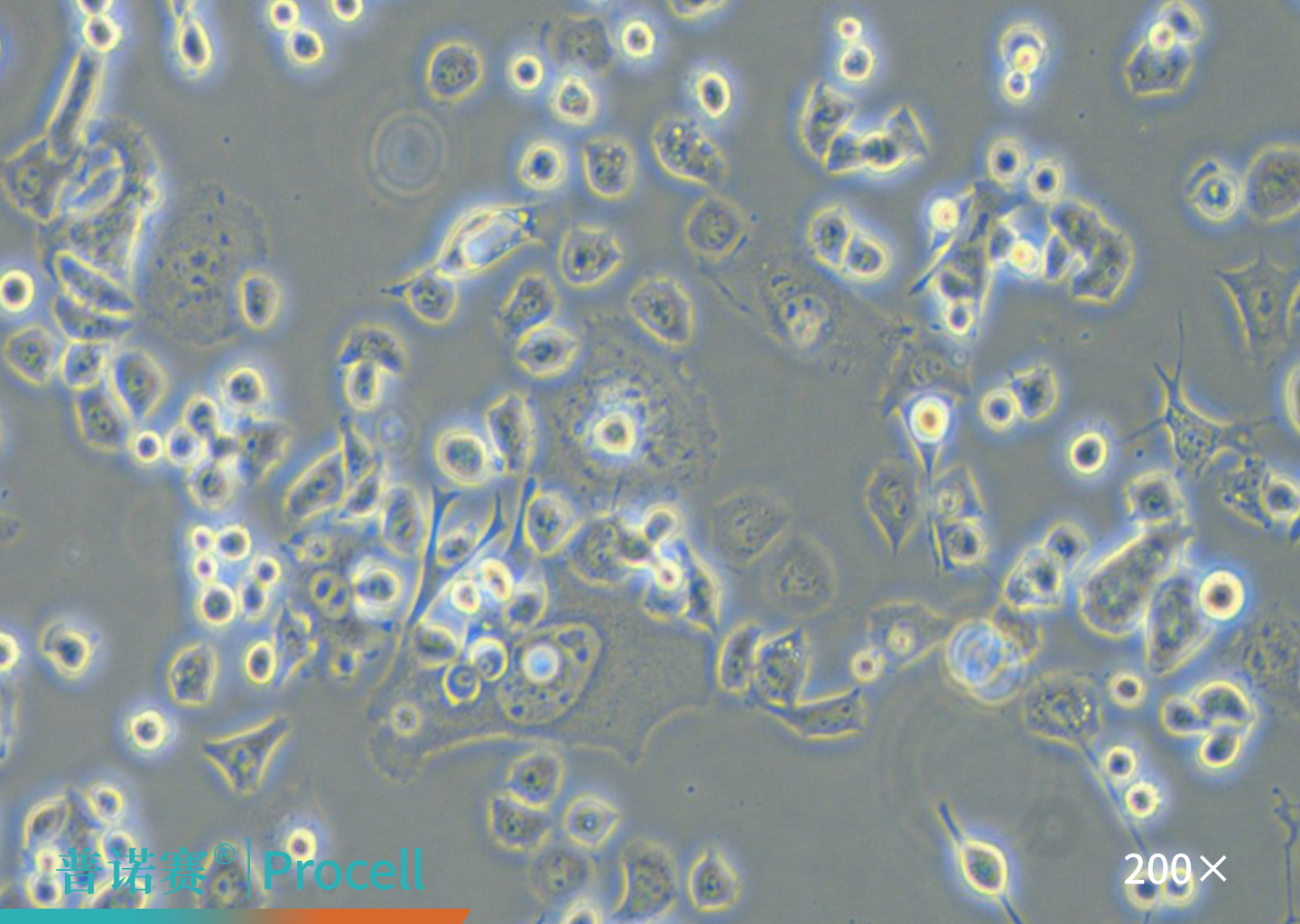 |
图2. Neuro-2a细胞的显微镜观察图
-
背景来源:
Neuro-2a细胞由R.J. Klebe和F.H. Ruddle从A系白化鼠的自发性肿瘤中建立。
-
应用场景:
Neuro-2a细胞产生大量微管蛋白,这种蛋白在轴浆流中发挥作用,调控神经细胞内物质运输。经过特定刺激(如秋水仙碱)诱导的Neuro-2a可作为体外模型,用于研究Tau或微管蛋白的异常代谢及相关信号通路变化,模拟AD神经元早期损伤状态。
-
培养方案:MEM(含NEAA)+10% FBS +1% P/S
-
培养要点:
1) 形态不均一,圆形细胞和带触角的多角形细胞的混合形态;
2) 生长较慢,1:2传代周期为3-4天。注意控制细胞密度不要过低;
3) 容易聚集堆叠生长,不会铺满瓶底,实际细胞密度比观察密度要大。
-
文献实例:
在秋水仙碱(OA)诱导的Neuro-2a细胞模型中,Lars2可以通过PI3K-AKT通路影响糖原合酶激酶3β (GSK3β)的表达,影响tau蛋白磷酸化和加重神经退行性变化[5]。
三、BV-2(小鼠小胶质细胞)
 |
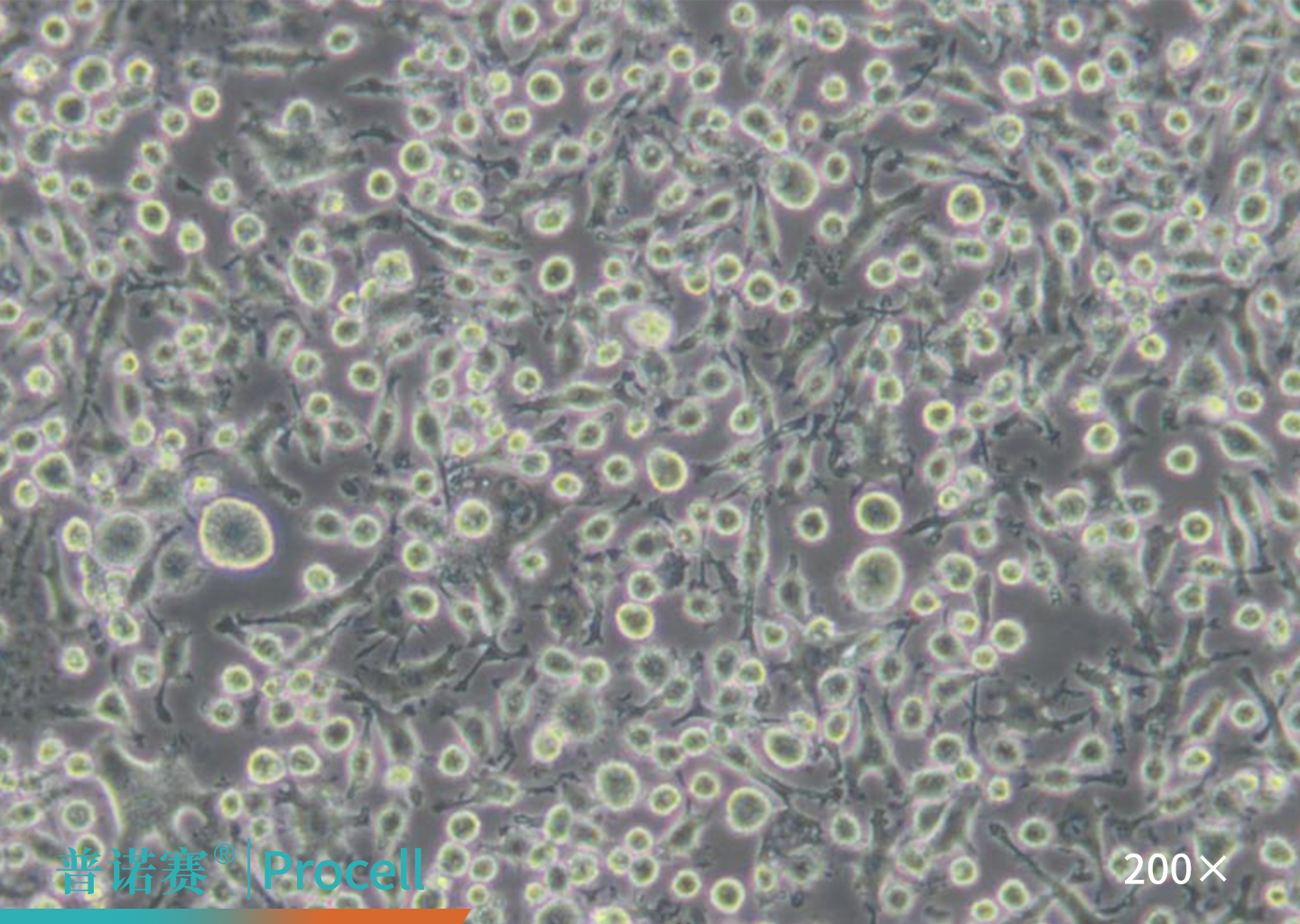 |
图3. BV-2细胞的显微镜观察图
-
背景来源:
BV-2细胞由E·Blasi于1990年建立,通过小鼠小神经胶质细胞经逆转录病毒介导转染v-raf/v-myc获永生化细胞系,保留小神经胶质细胞多种形态、表征和功能特征。
-
应用场景:
小胶质细胞是大脑主要免疫细胞,在机体对自体损伤或感染性因子的防御反应发挥关键作用。常与神经元细胞(如HT22)共培养,构建神经炎症-神经元损伤模型,以模拟AD体内环境[6]。
1) 半贴半悬,悬浮和贴壁细胞比例不固定;
2) 传代时注意单独收集悬浮和贴壁部分的细胞进行处理,贴壁部分需要用0.25%胰蛋白酶(含EDTA)消化;
3) 传代时需要保证细胞量,较低密度传代后,容易出现拉丝、触角较多的情况。
-
文献实例:
在BV-2和HT22细胞共培养模型中,Aβ25-35 刺激下,tRFAla-AGC-3-M8表达上调后,小胶质细胞和神经细胞中EphA7表达上调,并伴随着ERK1/2和p70S6K的磷酸化增加。通过抑制EphA7和增加tRFAla-AGC-3-M8的表达可抑制BV-2和HT22细胞中的ERK1/2-p70S6K信号通路,减轻了HT22细胞中的神经元损伤和tau过度磷酸化,并减少了由Aβ25-35诱导的BV-2细胞的M1型极化状态[6]。
四、HT22(小鼠海马神经元细胞)
 |
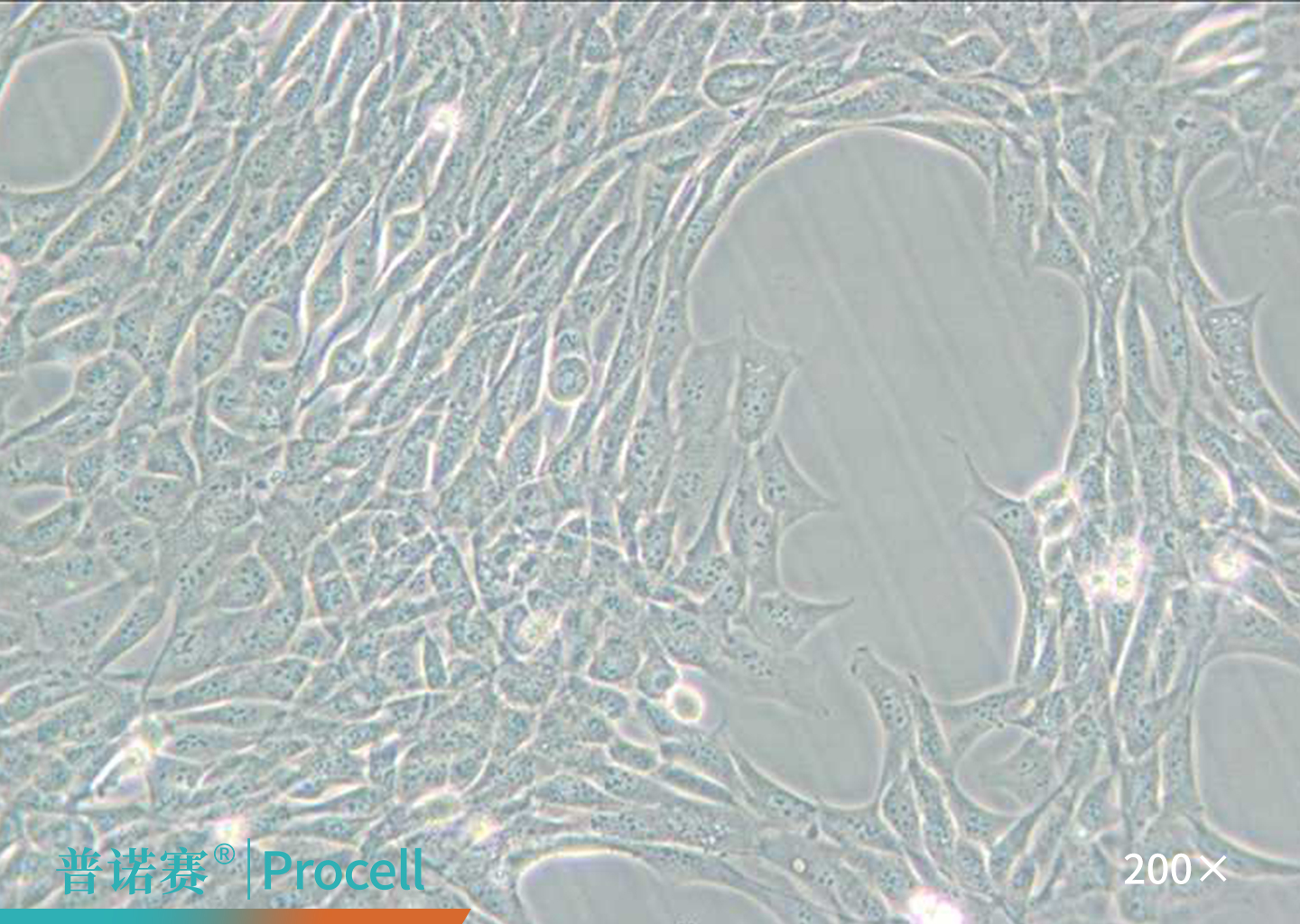 |
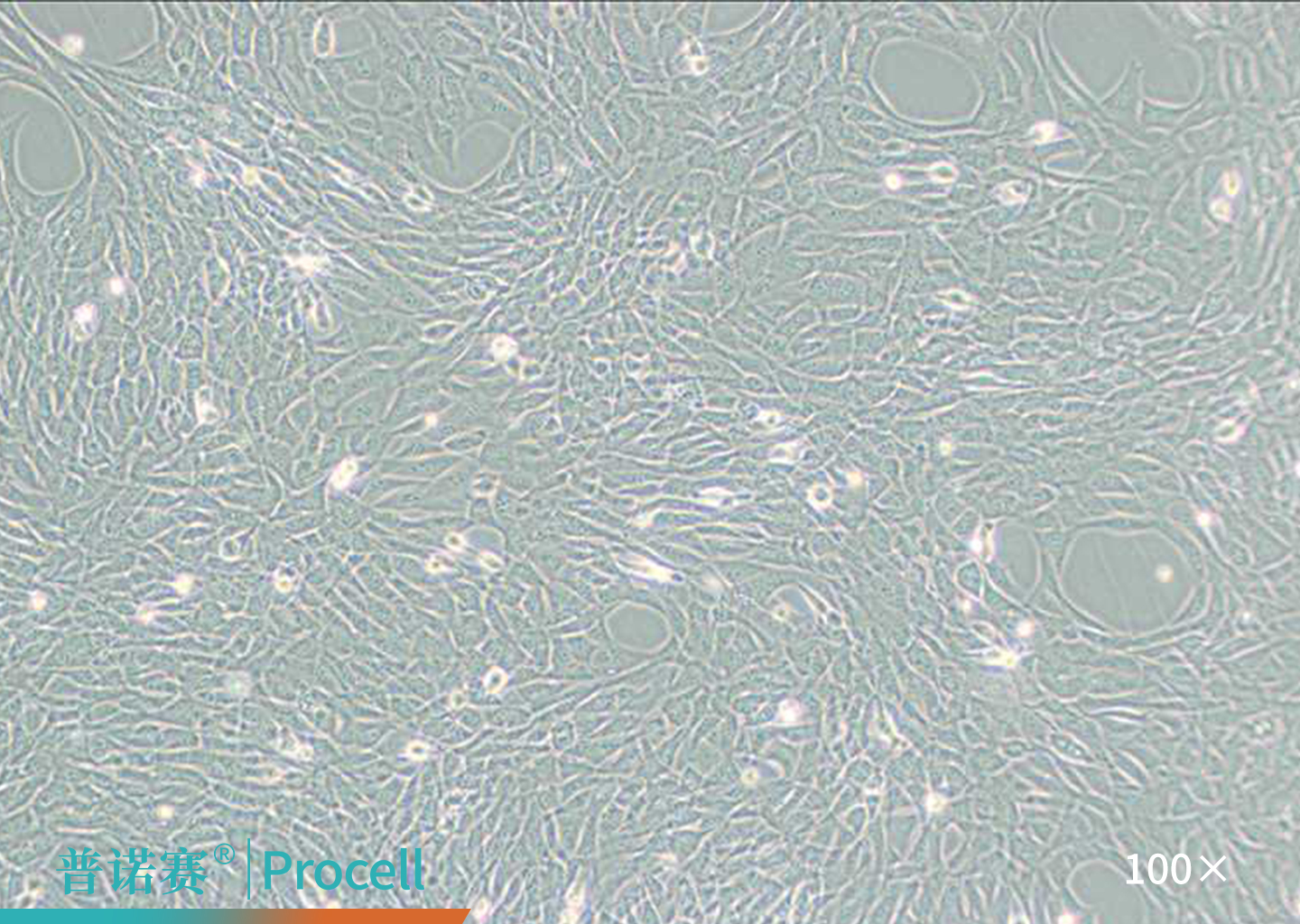
图4. HT22细胞的显微镜观察图
-
背景来源:
HT-22细胞是一种源自小鼠海马神经元细胞 HT4的亚克隆,在神经药理学研究中至关重要。
-
应用场景:
HT-22细胞表现出神经元表型,对谷氨酸高度敏感,基于这一特性,谷氨酸诱导的HT-22神经毒性模型已被认为是研究与神经退行性疾病包括AD相关的神经毒性的有价值的细胞模型。
1) 贴壁细胞,增殖较快;
2) 消化时注意观察消化状态,时间不宜过长,以免影响细胞活性。
-
文献实例:
3-羟基奎宁二酮作为铁死亡和单胺氧化酶B的双重抑制剂,在HT22细胞中评估了其抗铁死亡活性特性及在体内验证其可以降低与阿尔茨海默病相关的淀粉样前体蛋白和过度磷酸化tau蛋白[7]。
从AD病理机制的深度解析,到候选药物的初步验证,每一项研究突破的背后,都离不开稳定可靠的体外细胞模型作为基础支撑。普诺赛®凭借严格细胞系质控及专业的售前售后服务,不仅解决了体外实验中细胞一致性差、性能不稳定等痛点,同时为客户提供一对一的培养指导,为AD研究的每一步推进提供扎实工具保障。
除适配AD研究的核心细胞系外,普诺赛®还拥有SK-N-SH、PC-12等经典神经细胞系,满足不同神经退行性疾病研究。普诺赛®将持续以高性能细胞系产品,助力科研人员突破实验瓶颈,加速从基础研究到临床转化的进程,为最终破解阿尔茨海默病、帕金森病等难题注入可靠的“体外研究动力”。
相关产品推荐
| 产品名称 | 产品货号 | 产品规格 |
| SH-SY5Y [SHSY-5Y](人神经母细胞瘤细胞) | CL-0208 | 1×10^6Cells/T25 (常温)/1×10^6Cells/Vial×2Vials (冻存) |
| SH-SY5Y [SHSY-5Y]细胞专用培养基 | CM-0208 | 125mL×4 |
| Neuro-2a [N2a; Neuro-2a](小鼠脑神经瘤细胞) | CL-0168 | 1×10^6Cells/T25 (常温)/1×10^6Cells/Vial×2Vials (冻存) |
| BV2(小鼠小胶质细胞) | CL-0493 | 1×10^6Cells/T25 (常温)/1×10^6Cells/Vial×2Vials (冻存) |
| HT22(小鼠海马神经元细胞) | CL-0697 | 1×10^6Cells/T25 (常温)/1×10^6Cells/Vial×2Vials (冻存) |
| SK-N-SH(人神经母细胞瘤细胞) | CL-0214 | 1×10^6Cells/T25 (常温)/1×10^6Cells/Vial×2Vials (冻存) |
| MEM(含NEAA) | PM150410 | 500mL |
| DMEM高糖 | PM150210 | 500mL |
| 特级胎牛血清 | 164210 | 50mL×10/500mL/100mL/50mL |
| 青霉素-链霉素溶液(双抗),100× | PB180120 | 125mL |
参考文献:
1. Rumiana TenchoV, et al. Alzheimer’s Disease: Exploring the landscape of cognitive decline. ACS Chemical Neuroscience. 2024, 15, 3800-3827.
2. Targett IL, et al. Differentiation of SH-SY5Y neuroblastoma cells using retinoic acid and BDNF: a model for neuronal and synaptic differentiation in neurodegeneration. In Vitro Cellular & Developmental Biology-Animal. 2024 October;60(9):1058–1067.
3. Anchalee Prasansuklab, et al. Transcriptomic analysis of glutamate-induced HT22 neurotoxicity as a model for screening anti-Alzheimer’s drugs. Scientific Reports. 2023 May 4;13(1): 7225.
4. Dongsheng Ji, et al. Efficient strategy for alleviating neuronal apoptosis and oxidative stress damage of Alzheimer's disease through dual targeting BCL-2 gene promoter i-motif and β-amyloid. Redox Biology, 2025; 82: 103600.
5. Wenqi Qian, et al. Regulating Lars2 in mitochondria: A potential Alzheimer's therapy by inhibiting tau phosphorylation. Neurotherapeutics. 2024 April 4; 21 (4): e00353.
6. Zihao Deng, et al. tRFAla-AGC-3-M8 attenuates neuroinflammation and neuronal damage in Alzheimer's disease via the EphA7-ERK1/2-p70S6K signaling pathway. Alzheimer's Research & Therapy. 2025; 17 (1): 104.
7. Yangjing Lv, et al. 3-Hydroxyquinolin-2-Ones act as dual inhibitors of ferroptosis and monoamine oxidase B: reducing alzheimer’s disease-related amyloid precursor protein and hyperphosphorylated tau In vivo. Journal of Medicinal Chemistry. 2025; 68(13): 13661-13682.