武汉普诺赛生命科技有限公司品牌商
13 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
公司新闻/正文
解锁“宝藏”间充质干细胞MSCs:从特性解析到体外培养深度解析
395 人阅读发布时间:2025-10-21 11:01
间充质干细胞(Mesenchymal Stem Cell,MSCs)是一群成体干细胞。凭借其独特的生物学特性和显著的治疗潜能,MSCs已成为疾病研究领域的“新星”。截至2024年5月,全球范围内基于 MSCs 的在研临床试验已超1,200项,且已有超过27种MSCs相关产品获批,其临床应用价值已得到初步验证。
为帮助大家快速、系统地掌握MSCs关键知识,小普规划系列推文,依次介绍:MSCs概述、体外培养与扩增、三系分化和细胞治疗。
本期细胞学堂,小普将带大家了解MSCs的特性、功能、研究方向及体外培养策略,帮助您快速掌握这一研究前沿。
一. MSCs的基本特性
MSCs 来源于中胚层,具有高度的自我更新能力和多向分化潜能。其五大特性包括:自我复制、低免疫原性、高活性、趋炎性、不成瘤,这些特性使其在医学领域备受关注。
为规范MSCs 的研究与应用,国际细胞治疗学会(ISCT)提出了MSCs的定义标准,主要包括以下三个方面:
1. 贴壁性:在常规培养条件下,MSCs贴附于培养器皿表面生长。
2. 表面分子标志物:阳性表达CD105、CD73和CD90,同时阴性表达CD45、CD14或CD11b、CD79α或CD19以及HLA-DR。
3. 分化潜能:在体外条件下,MSCs能分化为成骨细胞、脂肪细胞和成软骨细胞。
注:随着研究的不断深入,ISCT提出的鉴定标准可能会进行更新。
MSCs可从骨髓、脐带、脂肪、牙齿、胎盘等多种组织中分离获取,在特定条件下可实现多向分化(图1)。
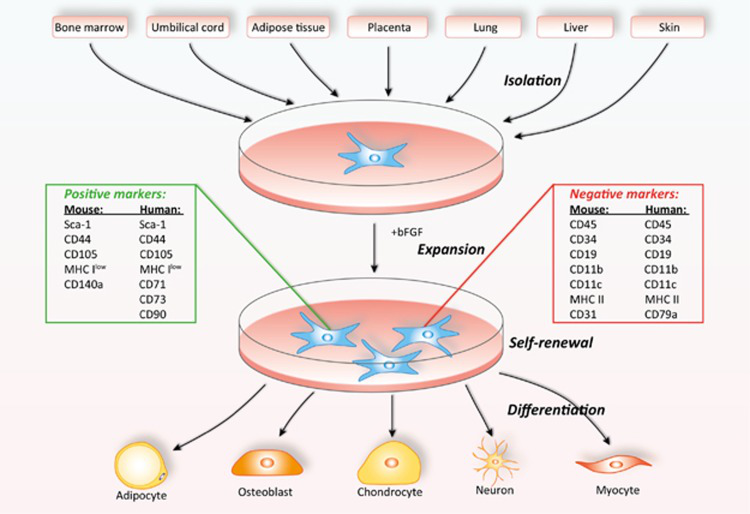
图1. MSCs的组织来源及分化潜能 图片引用文献[1]
不同来源的MSCs在细胞丰度、增殖能力及功能性上存在显著差异,这些差异影响了它们在不同研究和临床应用中的选择。常用来源MSCs的特点见表1。
表1. 常用来源MSCs特性分析
| 细胞名称 | 组织来源 | 核心特性 |
| 骨髓(BM-MSCs) | 骨髓穿刺液(侵入性操作) | 研究历史最长,分化潜能稳定,免疫调节机制明确,但数量有限,受年龄限制 |
| 脐带(UC-MSCs) | 新生儿脐带 | 来源丰富(产后废弃物),增殖能力强,免疫原性低 |
| 脂肪(AD-MSCs) | 脂肪组织(吸脂术获取) | 细胞产量高,易获取,增殖能力强,分化潜能低于BM-MSCs |
| 关节滑液(SF-MSCs) | 关节滑液(关节穿刺术) | 细胞数量少,具有一定的分化潜能和免疫调节作用 |
| 胎盘(P-MSCs) | 胎盘组织 | 来源丰富(产后废弃物),免疫调节能力强,增殖能力高 |
| 牙髓(DP-MSCs) | 牙髓 | 数量有限,受牙齿来源限制,增殖能力良好,神经分化潜能突出 |
二、MSCs的核心功能
MSCs 的临床价值主要依赖其四大核心功能,这些功能相互协同,为组织修复和疾病治疗提供支持:
1、自我更新和增殖能力
MSCs具有高度的自我更新和增殖能力,能够不断分裂产生新的干细胞,维持其数量和质量。
2、多向分化潜能
MSCs可以分化为多种细胞类型,包括成骨细胞、软骨细胞、脂肪细胞、心肌细胞、神经细胞等。
3、促进组织修复功能
MSCs通过分泌生长因子、免疫调节因子及构建支持性微环境,促进受损组织的再生和修复。
4、免疫调节特性
MSCs可调控免疫系统活性,抑制炎症反应,并在移植相关疾病中展现潜在疗效。
三、MSCs的研究应用
凭借多重功能,MSCs在多种临床前模型和疾病的临床试验中得到广泛探索[2-4],应用方向包括自身免疫性疾病、炎症性疾病、神经退行性疾病以及骨科损伤等(图2)。
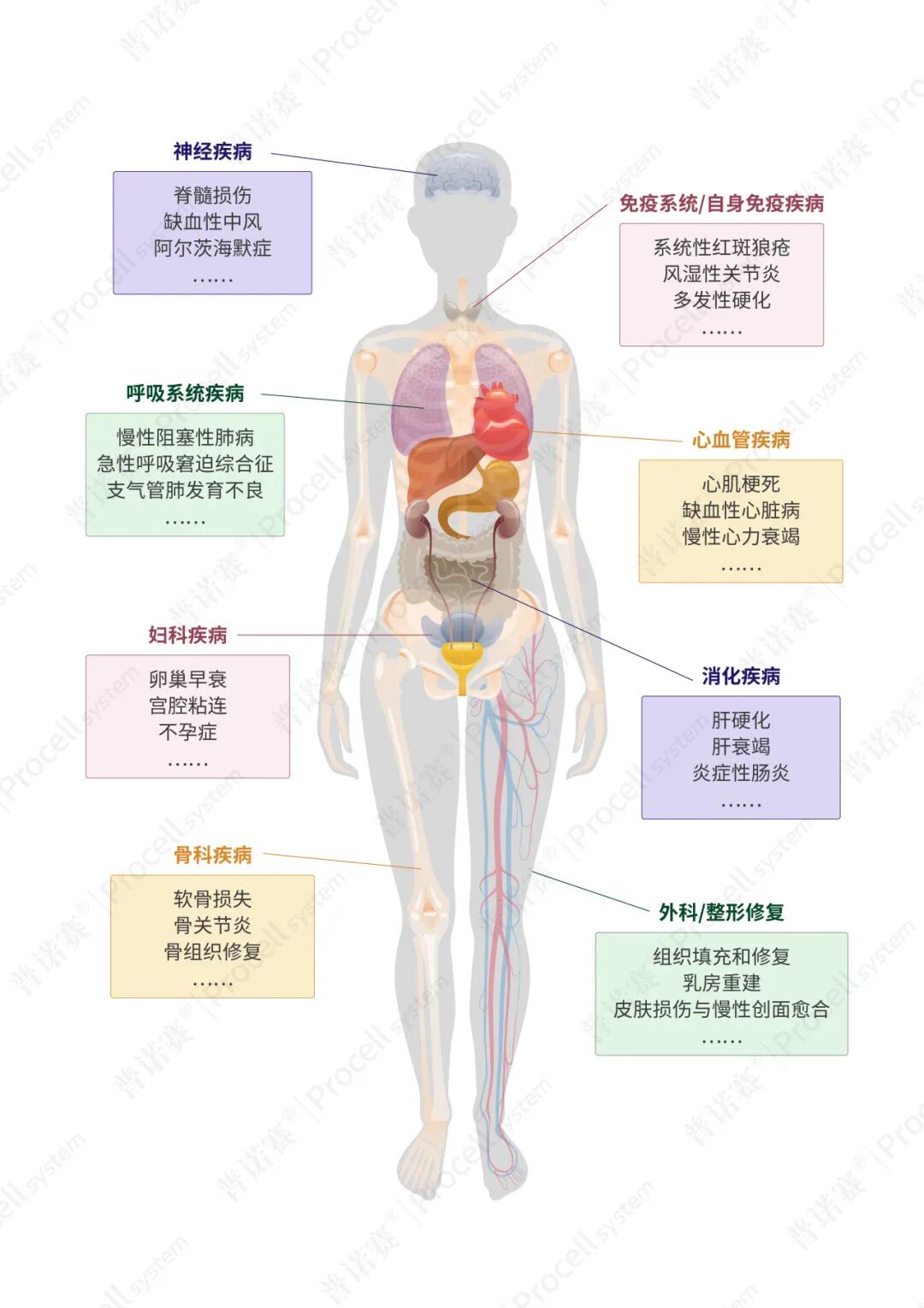
图2. MSCs在多种疾病中的应用方向
不同组织来源的MSCs在生物学特性、免疫调节能力及分化潜能等方面存在差异,这决定了它们在特定疾病治疗中的适用性和潜在优势。针对不同疾病选择适合来源的MSCs仍是研究热点[2-3](表2)。
表2. 主要来源MSC在疾病治疗中的应用及优势
| 细胞名称 | 应用领域 | 优势 |
| 骨髓(BM-MSCs) | 骨关节炎、脊髓损伤、移植物抗宿主病、肌萎缩侧索硬化症 (ALS),心血管疾病,内分泌紊乱,辅助生殖技术 | 免疫调节机制明确,长期安全性数据充足 |
| 脐带(UC-MSCs) | 心肌梗死、肝脏纤维化、神经退行性疾病 、呼吸系统疾病 | 免疫原性低,可实现 “异体移植”,来源不受年龄限制 |
| 脂肪(AD-MSCs) | 整形和美容手术(组织填充和修复,乳房重建)、关节炎和软骨损伤治疗、伤口愈合、自身免疫性疾病的治疗、心血管疾病 | 细胞产量高,成脂/成纤维分化能力强,适合软组织修复 |
四、MSCs体外培养策略
随着干细胞治疗需求不断增加,MSCs的体外扩增与培养体系显得尤为关键。选择适合的培养体系和培养方式,不仅可保持MSCs特性,还能提升其在临床上的应用价值。
1. 培养体系
常用的培养体系主要包括含血清培养基、无血清培养基以及含血清替代物培养基(表3)。
表3. MSCs体外培养体系分析
| 培养体系 | 优势 | 劣势 | 适用范围 |
| 含血清完全培养基 | 成本相对低,实验室普遍可用,细胞适应性强 | 批间差异大,存在临床风险 | 基础研究,常规细胞扩增 |
| 无血清培养基 | 化学成分明确、不含血清、无动物源、批间差异小,目标外泌体纯度高 | 价格较高,部分MSCs适应性差问题 | 外泌体研究,药物开发,临床应用 |
| 含血清替代物培养基 | 含血清替代物,模拟血清营养,规避血清风险,成本相对适中 | / | 科研研究 |
2. 培养方式
MSCs的培养方式主要包括二维(传统)和三维两种。
在二维培养中,细胞铺展在培养器皿的平面上生长,这种方法操作简便、成本较低,因而在再生医学及基础干细胞研究中仍被广泛应用。
然而,二维培养与体内的天然三维微环境存在明显差异。体外平面生长的MSCs容易出现形态改变、增殖动力学变化及分化潜能下降等问题。长期二维培养还可能导致多能性丧失、细胞提前衰老以及基因组稳定性降低。
为克服这些局限,研究者逐步发展了三维(3D)培养技术。3D培养通过无支架球体或基于水凝胶支架(如海藻酸盐、胶原、Matrigel等)的系统,为细胞提供更接近体内的立体微环境,使其在空间结构中实现自然的生长、增殖与迁移。
尽管三维培养操作更复杂、成本较高且标准化难度大,但其在模拟体内环境和维持MSCs生物学特性方面具有显著优势,应根据实验目的合理选择培养方式。
以上是关于间充质干细胞全面概览。后续小普还将带来间充质干细胞培养技巧、三系分化、细胞治疗等的精彩内容~
更多间充质干细胞内容详情,请持续关注细胞学堂专栏~
相关产品推荐
| 产品名称 | 产品货号 | 产品规格 |
| 小鼠骨髓间充质干细胞 | CP-M131 | 5×10^5Cells/T25 |
| 人脐带间充质干细胞 | CP-CL11 | 1×10^6Cells/T25 |
| 人脂肪间充质干细胞 | CP-H202 | 5×10^5Cells/T25 |
| 大鼠滑膜间充质干细胞 | CP-R304 | 5×10^5Cells/T25 |
| 更多产品推荐查看 | ||
参考文献
[1] Chen Q, Shou P, Zheng C, et al. Fate decision of mesenchymal stem cells: adipocytes or osteoblasts?. Cell Death & Differentiation. 2016; 23 (7): 1128-1139.
[2] Zhidu S, Ying T, Rui J, et al. Translational potential of mesenchymal stem cells in regenerative therapies for human diseases: challenges and opportunities. Stem Cell Research & Therapy. 15, 266 (2024).
[3] Zhou J, Shi Y, et al. Mesenchymal stem/stromal cells (MSCs): origin, immune regulation, and clinical applications. Cellular & Molecular Immunology. 20, 555–557 (2023).
[4] Han X, Liao R, Li X, et al. Mesenchymal stem cells in treating human diseases: molecular mechanisms and clinical studies. Signal Transduction and Targeted Therapy. 10, 262 (2025).
[5] Li J, Wu Z, Zhao L, et al. The heterogeneity of mesenchymal stem cells: an important issue to be addressed in cell therapy. Stem Cell Research & Therapy. 2023; 14 (1): 381.
[6] Moldaschl J, Chariyev-Prinz F, Toegel S, et al. Spheroid trilineage differentiation model of primary mesenchymal stem/stromal cells under hypoxia and serum-free culture conditions. Frontiers in Bioengineering and Biotechnology. 2024; 12: 1444363.
[7] Bicer M, Cottrell GS, Widera D. Impact of 3D cell culture on bone regeneration potential of mesenchymal stromal cells. Stem Cell Research & Therapy. 2021; 12 (1): 31.