武汉普诺赛生命科技有限公司品牌商
13 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
公司新闻/正文
A549细胞mRNA转染实操干货,解锁高效、低毒的转染解决方案
91 人阅读发布时间:2026-03-19 09:19
在生物医学研究领域,mRNA转染技术正凭借其独特的优势重塑基因功能研究的范式。A549细胞作为重要的人非小细胞肺癌模型,在癌症研究、药物筛选和毒理学评估中具有不可替代的价值。然而,传统的mRNA转染在A549细胞中常面临转染效率低、细胞毒性大等挑战。本期细胞学堂聚焦A549转染核心难题,分享经实测验证的A549细胞mRNA转染实操干货,解锁高效、低毒的转染解决方案。
一、A549细胞概况
A549细胞系是一种常用的人类非小细胞肺癌细胞系,由D.J. Giard等人于1972年通过一个58岁白人男性的肺癌组织建立。A549细胞能够利用胞苷二磷酸胆碱途径合成具有高百分比去饱和脂肪酸的卵磷脂,形态上呈上皮细胞样,具有贴壁生长的特性。在体外培养时通常以单层细胞形式贴壁生长,倍增时间约为22 h,适合作为转染的宿主细胞。
1、基本信息
组织来源:肺癌
细胞类型:肿瘤细胞
生长特性:贴壁细胞
细胞形态:上皮细胞样
2、培养方案
生长培养基:Ham's F-12K+10% FBS+1% P/S
培养条件:气相:空气,95%;CO2,5%;温度:37℃
推荐传代比例:1:3-1:6
推荐换液频率:2-3次/周
二、A549细胞应用及研究进展
1、药物筛选
A549细胞被用于药物筛选,是开发新型肺癌治疗药物的重要模型之一。通过研究其对药物的敏感性,可为肺癌的个体化治疗提供重要参考。
2、机制研究
通过研究A549细胞的致癌和转移机制,可以深入了解非小细胞肺癌的发病过程及分子调控机制,为肺癌治疗的研究提供理论基础。
3、靶向治疗
A549细胞常用于探索KRAS等关键信号通路及其调控机制,为发现肺癌特定治疗靶点提供实验依据。
4、免疫治疗
A549细胞作为非小细胞肺癌的典型细胞模型,常用于研究PD-L1等免疫检查点的表达调控及药物机制,为免疫治疗的研究提供实验支持。
5、新型药物研发
针对肺癌的药物研究不断取得新进展,研究者通过实验,人工合成小分子及大分子化合物,然后在A549细胞中验证药物的作用机制。
在这些研究中,基因转染是常用的实验手段,可通过基因编辑、沉默或过表达,从而调控与疾病相关的蛋白质水平,揭示疾病机制。随着技术的进步,研究人员对高效、低毒转染体系的需求日益增加,这也正是A549细胞专用mRNA转染试剂开发的直接动力。
三、Mergene1000® A549 [A-549]细胞专用mRNA转染试剂使用指南
接种细胞(以24孔板为例)
-
转染前24 h接种细胞于孔板中,待细胞汇合度达70-90%时开始转染。
转染复合物制备
-
转染试剂稀释:取0.6 μL Mergene1000®A549 [A-549]细胞专用mRNA转染试剂加入50 μL Ham's F-12K培养基中。
-
mRNA稀释:取0.2 μg mRNA,加入上述转染试剂稀释液中(转染试剂(μL):mRNA(μg)=3:1)。
-
复合物孵育:将上述稀释液室温静置5-10 min。
转染培养及检测
-
复合物添加:将制备好的转染复合物逐滴加到细胞液中。
-
细胞培养:采用8字法混匀细胞培养板,放置于37℃,5% CO2培养箱中培养。
-
转染培养12-24 h后可检测基因表达。
表1. A549细胞不同培养容器转染参考用量
| 培养器皿 | 单孔面积 | 细胞接种量 | 接种培养基 | 基础培养基 | mRNA转染 | |
| 稀释后终体积 | 试剂用量 | mRNA | ||||
| 96孔板 | 0.3 cm2 | 1-4×104个/孔 | 200 μL | 10 μL | 0.3 μL | 0.1 μg |
| 24孔板 | 2.0 cm2 | 0.8-1.2×105个/孔 | 500 μL | 50 μL | 0.6 μL | 0.2 μg |
| 12孔板 | 4.0 cm2 | 1.6-2.4×105个/孔 | 1 mL | 100 μL | 1.2 μL | 0.4 μg |
| 6孔板 | 10.0 cm2 | 4-6×105个/孔 | 2 mL | 200 μL | 3.0 μL | 1.0 μg |
| 6 cm | 20.0 cm2 | 0.8-1.2×106个/孔 | 5 mL | 0.5 mL | 6.0 μL | 2.0 μg |
| 10 cm | 60.0 cm2 | 2.4-3.6×106个/孔 | 15 mL | 1.0 mL | 18.0 μL | 6.0 μg |
(注:该表使用量仅供参考,转染试剂实际使用量还需根据细胞状况及其他实验条件优化。)
转染效果展示
-
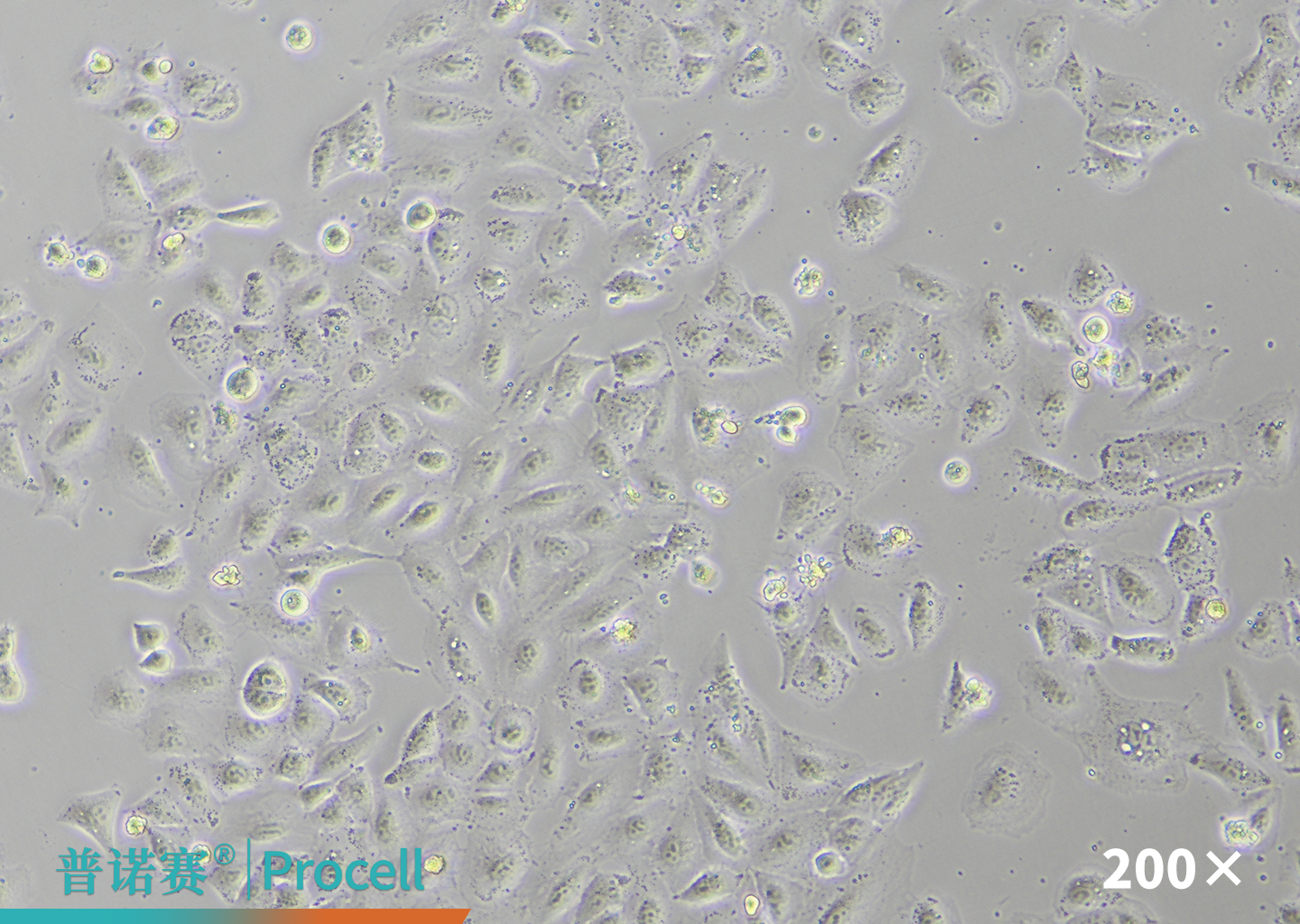
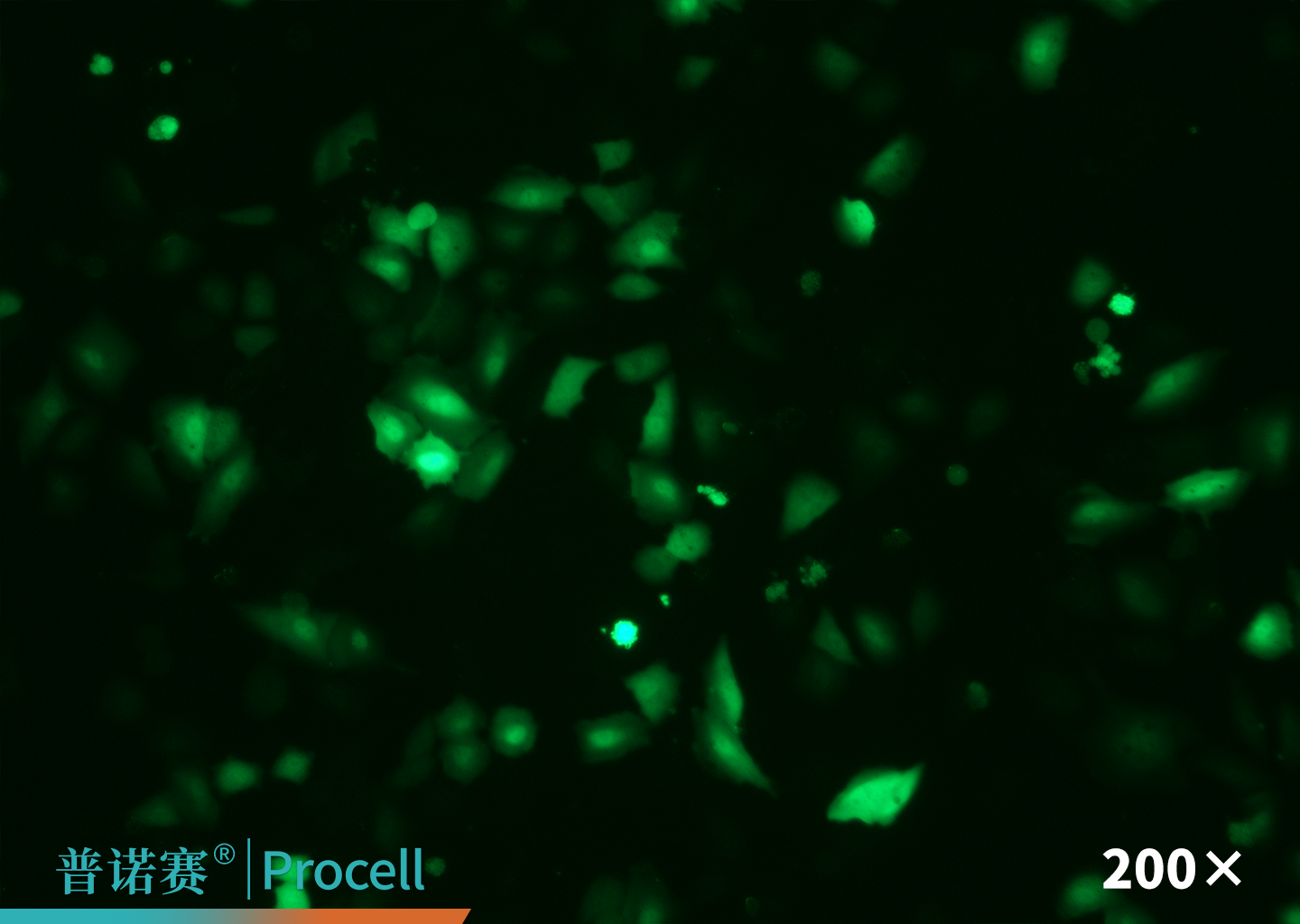
分别使用Mergene1000® A549 [A-549]细胞专用mRNA转染试剂和T品牌L3000转染试剂,将EGFP-mRNA转染至A549细胞中。
-
实验结果显示:Mergene1000® 在A549细胞中的转染效率可达80%以上,显著高于传统mRNA转染,且优于T品牌L3000转染试剂。
| Mergene1000® vs T品牌L3000 | ||
| 白光图片 | ![Mergene1000® A549 [A-549]细胞专用mRNA转染试剂白光图片](https://files.procell.com.cn/article-imgs/A549-1.png) |
 |
| 荧光图片(EGFP) | ![Mergene1000® A549 [A-549]细胞专用mRNA转染试剂荧光图片](https://files.procell.com.cn/article-imgs/A549-3.png) |
 |
| 流式检测(转染效率) | ![Mergene1000® A549 [A-549]细胞专用mRNA转染试剂流式检测图](https://files.procell.com.cn/article-imgs/A549-5.png) |
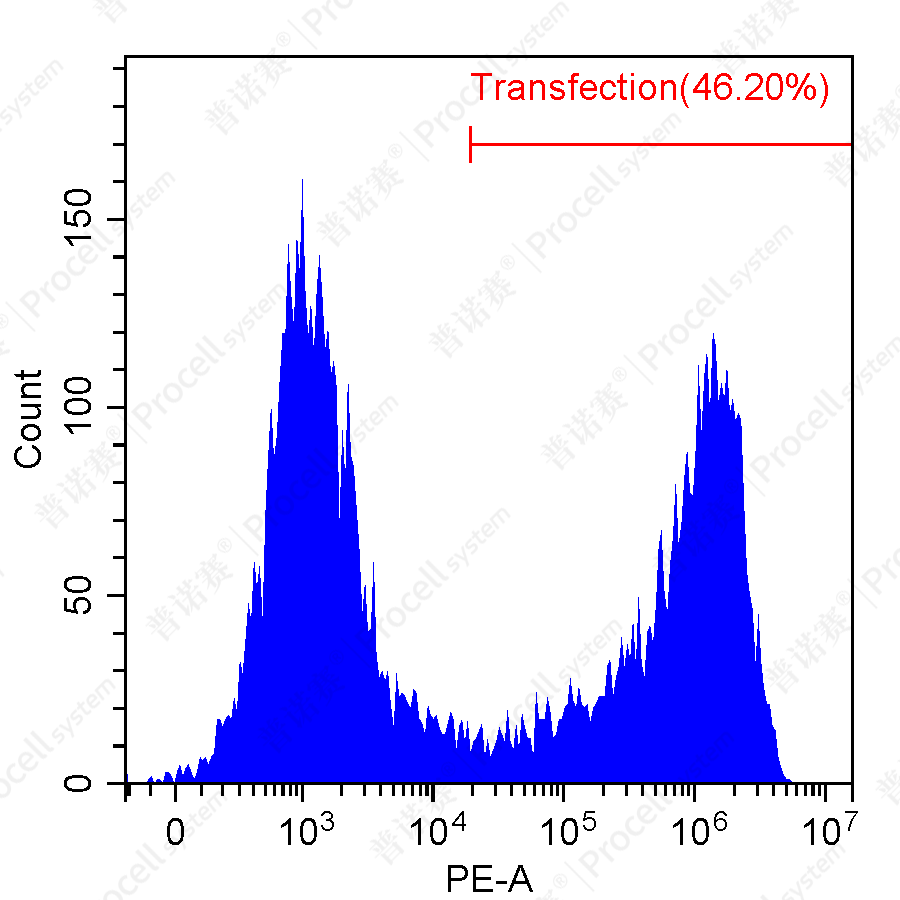 |
图1. A549细胞转染效率检测
(注:实验同步进行,转染条件均按照各品牌说明书执行,结果仅供参考)
四、常见问题解答(FAQs)
Q:转染A549细胞是否需要无血清培养基?
A:不是必须全程无血清,但转染复合物制备时必须用无血清培养基(如Ham's F-12K培养基),而细胞在转染前、后都可以放在含血清的完全培养基里。使用Mergene1000® A549细胞专用mRNA转染试剂转染后可根据细胞状态,培养4-6 h选择是否更换培养基。
Q:如何提高mRNA在A549细胞中的稳定性?
A:①使用经过核苷酸修饰的mRNA(如假尿苷修饰),优化5'和3'非翻译区(UTR)序列。
②避免RNase污染。
Q:如何提高转染效率以及避免转染后细胞死亡?
A:①建议使用对数生长期、活力良好的细胞进行转染,避免使用传代次数过多或受到污染的细胞,控制细胞汇合度在70%-90%。
②使用高纯度的mRNA有助于获得较高的转染效率。
③可根据实际情况尝试降低核酸或转染试剂用量,转染后培养4-6 h更换新鲜培养基。
A549细胞专用mRNA转染试剂凭借高效率、低毒性、快速表达和稳定性好的特点,成为基因功能研究、药物筛选和信号通路分析的理想工具。
以上是关于Mergene1000® A549细胞转染的高效解决方案与实操干货,拆解核心技巧与避坑要点~更多细胞培养干货,请持续关注细胞学堂专栏~
了解更多细胞类型的转染解决方案,请点击转染试剂,查看全系列产品。
| 货号 | 产品名称 | 规格 |
| 164427 | Mergene1000® A549 [A-549]细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164423 | Mergene1000® Vero细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164413 | Mergene1000® Vero细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164435 | Mergene1000® THP-1细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164430 | Mergene1000® RAW 264.7细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164425 | Mergene1000® NIH/3T3细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164415 | Mergene1000® NIH/3T3细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164434 | Mergene1000® MCF7 [MCF-7]细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164432 | Mergene1000® MCF7 [MCF-7]细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164426 | Mergene1000® Hep G2细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164416 | Mergene1000® Hep G2细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164424 | Mergene1000® Hela细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164414 | Mergene1000® Hela细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164433 | Mergene1000® COS-7细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164431 | Mergene1000® COS-7细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164428 | Mergene1000® CHO-K1细胞专用mRNA转染试剂 | 100μL / 0.5mL / 1mL |
| 164418 | Mergene1000® CHO-K1细胞专用DNA转染试剂 | 100μL / 0.5mL / 1mL |
参考文献:
[1] Giard DJ, Aaronson SA. In vitro cultivation of human tumors: establishment of cell lines derived from a series of solid tumors. Journal of the National Cancer Institute. 1973 November;51 (5): 1417-23.
[2] Nelson-Rees WA, Flandermeyer RR. Distinctive banded marker chromosomes of human tumor cell lines. International Journal of Cancer. 1975 July 15;16 (1): 74-82.
[3] Lieber M, Smith B. A continuous tumor-cell line from a human lung carcinoma with properties of type II alveolar epithelial cells. International Journal of Cancer. 1976 January 15; 17 (1): 62-70.
[4] Chary A. Culturing human lung adenocarcinoma cells in a serum-free environment. Methods in Molecular Biology. 2023; 2645: 165-172.
[5] Francisco Junior RDS, Temerozo JR. Differential haplotype expression in class I MHC genes during SARS-CoV-2 infection of human lung cell lines. Frontiers in Immunology. 2023 February 1; 13: 1101526.
[6] Rezaei I, Sadeghi A. The effects of cetuximab and cisplatin anti-cancer drugs on the mechanical properties of the lung cancerous cells using atomic force microscope. Biochemistry and Cell Biology. 2023 December 1; 101 (6): 531-537.